- 哈工大李玲教授、張明宇副教授聯(lián)合研究成果為
- 湖南大學(xué)物電院羅海陸/文雙春教授團(tuán)隊(duì)提出并
- 南京理工大學(xué)電光學(xué)院陳錢、左超教授團(tuán)隊(duì)在計(jì)
- 英國(guó)新建散射掃描近場(chǎng)光學(xué)顯微鏡設(shè)施
- 西安光機(jī)所計(jì)算光學(xué)顯微成像研究獲進(jìn)展
- 拒絕進(jìn)口,湖南省人民醫(yī)院600采購P3實(shí)驗(yàn)室儀
- 市場(chǎng)月報(bào)丨十二月非光學(xué)顯微鏡中標(biāo)盤點(diǎn)
- 市場(chǎng)月報(bào)丨九月非光學(xué)顯微鏡中標(biāo)盤點(diǎn)出爐
- 蘇州市藥檢中心預(yù)算1073萬元采購一批儀器設(shè)備
- 科學(xué)家研發(fā)新材料 能大幅提升光學(xué)顯微鏡的分
- 凡本網(wǎng)注明"來源:儀表網(wǎng)"的所有作品,版權(quán)均屬于儀表網(wǎng),未經(jīng)本網(wǎng)授權(quán)不得轉(zhuǎn)載、摘編或利用其它方式使用上述作品。已經(jīng)本網(wǎng)授權(quán)使用作品的,應(yīng)在授權(quán)范圍內(nèi)使用,并注明"來源:儀表網(wǎng)"。違反上述聲明者,本網(wǎng)將追究其相關(guān)法律責(zé)任。
- 本網(wǎng)轉(zhuǎn)載并注明自其它來源的作品,目的在于傳遞更多信息,并不代表本網(wǎng)贊同其觀點(diǎn)或證實(shí)其內(nèi)容的真實(shí)性,不承擔(dān)此類作品侵權(quán)行為的直接責(zé)任及連帶責(zé)任。其他媒體、網(wǎng)站或個(gè)人從本網(wǎng)轉(zhuǎn)載時(shí),必須保留本網(wǎng)注明的作品來源,并自負(fù)版權(quán)等法律責(zé)任。
- 如涉及作品內(nèi)容、版權(quán)等問題,請(qǐng)?jiān)谧髌钒l(fā)表之日起一周內(nèi)與本網(wǎng)聯(lián)系,否則視為放棄相關(guān)權(quán)利。
- 合作、投稿、轉(zhuǎn)載授權(quán)等相關(guān)事宜,請(qǐng)聯(lián)系本網(wǎng)。聯(lián)系電話:0571-87759945,QQ:1103027433。
-
長(zhǎng)光辰芯登陸港交所主板 募資總額約26.04億港元
2通富微電2025年凈利潤(rùn)12.19億元 同比增長(zhǎng)79.86%
3信捷電氣2025年凈利潤(rùn)同比增長(zhǎng)11.21% 擬10派9.5元
5川儀股份2025年度歸母凈利潤(rùn)6.43億元 擬10派2.1元
6寧水集團(tuán)2025年度歸母凈利潤(rùn)約9335萬元,同比增長(zhǎng)78.09%
7三川智慧2025年歸母凈利潤(rùn)1.42億元,同比增長(zhǎng)122.80%
8佰維存儲(chǔ)2026年一季度凈利潤(rùn)28.99億元,扭虧為盈
9合肥智能傳感器產(chǎn)業(yè)園項(xiàng)目加快推進(jìn) 賦能千億產(chǎn)業(yè)集群建設(shè)?
10841.32萬元,恩施州農(nóng)科院農(nóng)博園建設(shè)項(xiàng)目科創(chuàng)中心實(shí)驗(yàn)室儀器設(shè)備采購招標(biāo)
-
11柯力傳感戰(zhàn)略投資新港電子 進(jìn)一步完善MEMS傳感布局?
122026年Q1色譜、質(zhì)譜類儀器招標(biāo)采購數(shù)據(jù)分析:進(jìn)口主導(dǎo),國(guó)產(chǎn)突圍
13中國(guó)科學(xué)院西安光機(jī)所在高功率摻鐿光纖領(lǐng)域取得重要進(jìn)展
14科遠(yuǎn)智慧2026年一季度營(yíng)收4.45億元,凈利潤(rùn)7624.86萬元
15燦瑞科技計(jì)劃斥資1600萬至3200萬元回購公司股份
162026年一季度國(guó)民經(jīng)濟(jì)實(shí)現(xiàn)良好開局
172026年3月份規(guī)模以上工業(yè)增加值增長(zhǎng)5.7%
18偉創(chuàng)電氣2025年度歸母凈利潤(rùn)2.63億元,擬10派3.5元
-
21科達(dá)自控下修2025年業(yè)績(jī):虧損9012萬元
22日聯(lián)科技今起停牌 擬購買上海菲萊測(cè)試公司控股權(quán)
23拓邦股份2025年?duì)I收110.82億元,歸母凈利潤(rùn)3.64億元
24556萬元,河南農(nóng)業(yè)大學(xué)家禽創(chuàng)新平臺(tái)基礎(chǔ)設(shè)備采購項(xiàng)目公開招標(biāo)
25市場(chǎng)監(jiān)管總局發(fā)布24項(xiàng)國(guó)家計(jì)量技術(shù)規(guī)范 多領(lǐng)域迎來精準(zhǔn)計(jì)量新保障
26海爾入主成效初顯,新時(shí)達(dá)2025年凈利潤(rùn)550.77萬元
27“長(zhǎng)江系”受讓山科智能股權(quán)未果,控制權(quán)變更落空后7%股份交易亦終止
28科遠(yuǎn)智慧擬斥資14億元開展現(xiàn)金管理 提升資金效能賦能股東回報(bào)?
-
鄭州長(zhǎng)城科工貿(mào)有限公司 面議
-
整體開關(guān)型部分回轉(zhuǎn)電動(dòng)執(zhí)行器
江蘇貝爾閥門控制有限公司 ¥ 2680 -
山東仁科測(cè)控技術(shù)有限公司 ¥ 89
-
山東瑤安電子科技發(fā)展有限公司 面議
-
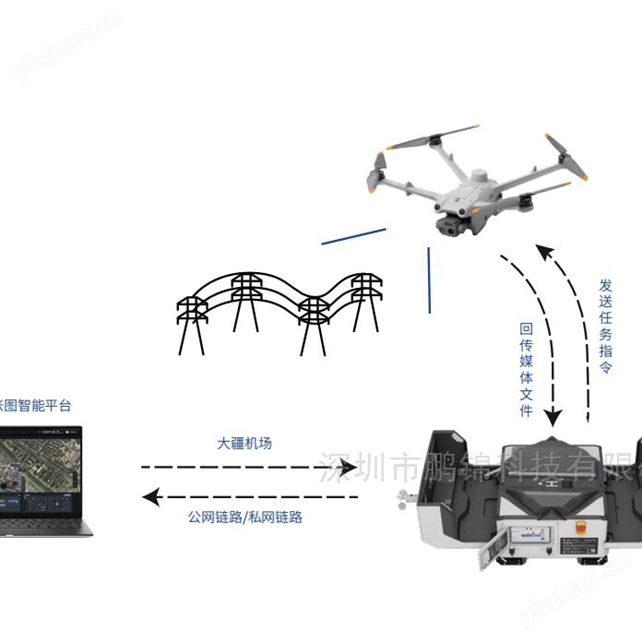
鵬錦智飛無人機(jī)管理平臺(tái)無人值守遠(yuǎn)程調(diào)度
深圳市鵬錦科技有限公司 面議



















所有評(píng)論僅代表網(wǎng)友意見,與本站立場(chǎng)無關(guān)。