-
 儀表網手機版
儀表網手機版
手機訪問更快捷
 儀表網小程序
儀表網小程序
更多流量 更易傳播
-
 公眾號:ybzhan
公眾號:ybzhan
隨時掌握行業動態
 掃碼關注視頻號
掃碼關注視頻號
網絡課堂 行業直播
在 3D 細胞培養技術飛速發展的今天,類器官憑借其模擬體內器官結構與功能的優勢,成為研究發育、疾病機制及藥物篩選的核心模型。
然而,類器官的三維結構也為觀測帶來挑戰 —— 傳統切片成像破壞樣本完整性,常規顯微鏡難以穿透厚樣本。
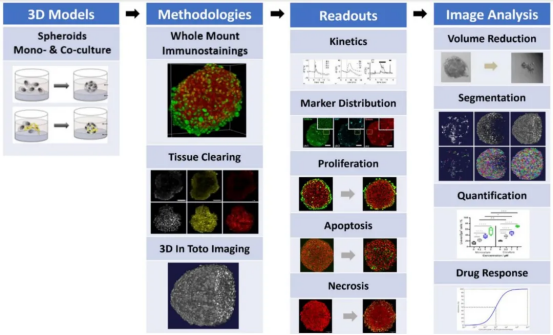
“類器官 + 組織透明化 + 光片顯微鏡” 的技術組合,恰好破解了這一難題。本文結合三篇核心文獻,從文獻簡介、組織透明化方法、光片成像方案、分析結果四個維度,詳細拆解這項技術的落地應用,為科研人員提供實用參考。
腫瘤類器官藥物篩選 —— 單細胞水平解析藥物療效差異
01文獻簡介
發表于《BMC Cancer》(2024)的《A spheroid whole mount drug testing pipeline with machine-learning based image analysis identifies cell-type specific differences in drug efficacy on a single-cell level》,聚焦腫瘤微環境中 “腫瘤細胞 - 成纖維細胞” 相互作用對藥物響應的影響。研究團隊構建了 KP-4 胰腺癌細胞與 CCD-1137Sk 成纖維細胞的共培養類器官模型,開發了一套從類器官制備、透明化、3D 成像到深度學習分析的完整流程,在單細胞水平揭示了不同細胞類型對藥物的差異性響應。

02組織透明化方法
該研究針對腫瘤類器官(直徑可達 500μm)的厚樣本特性,采用甘油基光學透明化技術,具體步驟如下:
1.樣本預處理:類器官經 4% 多聚甲醛(PFA)固定 1 小時后,用含 1% 胎牛血清(FBS)的 PBS 清洗,再用 0.5M 淬滅殘留固定劑,避免熒光信號干擾。
2.滲透增強:將類器官置于含 0.2% Triton X-100、0.3M 、20% DMSO 的穿透緩沖液中孵育 30 分鐘,為后續抗體滲透和透明化試劑擴散鋪路。
3.透明化處理:可平衡類器官內部與外部環境的折射率,顯著降低光散射,確保激光能穿透 500μm 厚的類器官,同時避免樣本收縮或變形。
4.驗證環節:通過對比 “透明化類器官的光學切片” 與 “傳統冷凍切片” 的熒光信號(Ki-67 增殖標記、Cleaved Caspase-3 凋亡標記),證明透明化后不同深度(50μm、250μm、500μm)的細胞標記率與冷凍切片無顯著差異,驗證了透明化的可靠性。
03成像方法
樣本掛載:透明化后的類器官置于含 88% 甘油的 Ibidi μ-slide 中,平衡溫度后成像,避免樣本移動或脫水。
成像參數:采用 20× 水浸物鏡(NA 0.75),激光波長覆蓋 405nm(DRAQ5 核染)、488nm(熒光抗體)、561nm(壞死標記),z 軸步長 1μm,激光強度控制在 1-2% 以減少光毒性,同時開啟 z 補償功能,抵消深度依賴的信號衰減。
數據兼容性:也可適配光片顯微鏡的多視角成像需求 —— 若改用光片顯微鏡,僅需調整樣本掛載方式(如 FEP 管固定),即可實現更快的成像速度。
04分析結果
類器官生長與藥物響應特征:
共培養類器官(KP-4+CCD-1137Sk)比 KP-4 單培養類器官生長更快,處理后,總細胞數仍高于單培養組,初看似乎 “共培養增強耐藥性”。
但單細胞水平分析揭示:成纖維細胞是耐藥核心——CCD-1137Sk 成纖維細胞對兩種藥物的耐受性顯著高于 KP-4 腫瘤細胞,說明共培養未增強腫瘤細胞耐藥性,反而可能通過旁分泌信號增加其敏感性。

空間分布特征:
通過 3D 殼層分析(將類器官分為內、中、外三層),發現未處理組中 90% 的增殖細胞(Ki-67+)位于中外層,50-60% 的凋亡細胞位于核心;藥物處理后,共培養類器官核心區域的增殖細胞減少更顯著,而單培養類器官的凋亡細胞主要集中在外層,提示微環境影響藥物在類器官內的滲透與作用。

乳腺類器官動態觀測 ——
光片顯微鏡追蹤發育與信號變化
01文獻簡介
發表于《Journal of Mammary Gland Biology and Neoplasia》(2025)的《Live-cell imaging of mammary organoids using light sheet microscopy》,針對乳腺類器官的動態發育研究需求,優化了 “類器官培養 - 透明化 - 光片成像” 的全流程。研究以小鼠乳腺類器官(含 EKAREV-NLS 熒光報告基因或 H2B-mCherry 核標記)為模型,開發了多視角和倒置兩種光片顯微鏡的樣本掛載方案,實現長達 72 小時的低光毒性實時成像,清晰捕捉乳腺類器官分支形態發生、細胞增殖及信號分子動態變化,為乳腺發育生物學提供了全新觀測工具。

02組織透明化方法
考慮到乳腺類器官(部分為囊性結構)的脆弱性,研究采用溫和透明化策略,避免破壞樣本完整性:
1.類器官包埋:若需長期存儲或高分辨率成像,采用Matrigel / 膠原 I 基質保留策略—— 類器官嵌入含 15mg/mL 基底膜提取物(BME)和 1.5mg/mL 膠原 I 的 3D 基質。
2.類器官組織透明化:僅用少量 88% 甘油浸潤,既維持基質結構,又輕度降低光散射,透明化后樣本可在 4℃存儲 1 周,-20℃存儲 6 個月。
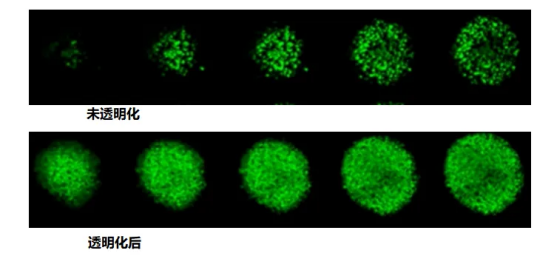
3.關鍵驗證:對比 “無透明化活細胞成像” 與 “透明化固定成像” 的 Ki-67 標記率,兩者無顯著差異(活細胞組 54.37±1.68% vs 透明化組 47.44±1.98%),證明透明化不影響細胞狀態評估。
03光片顯微鏡成像方法
研究核心采用多視角光片顯微鏡(ZEISS Lightsheet 7)和倒置光片顯微鏡(Luxendo TruLive3D),針對不同乳腺類器官類型設計專屬方案:
1. 多視角光片顯微鏡(適用于大體積乳腺類器官,直徑 > 300μm)
樣本掛載:類器官嵌入 FEP 管(內徑 1.3mm,壁厚 0.15mm)中的 ECM 凝膠柱,垂直懸掛。
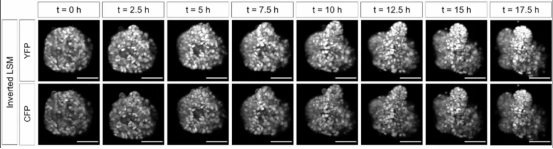
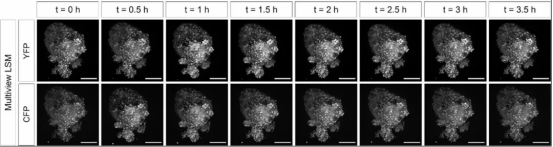
成像參數:采用 10× 和 20× 檢測物鏡,光片厚度 6μm,多視角(4 個角度)成像后拼接,z 軸步長 2μm。
優勢:可捕捉類器官 360° 全景,解決大體積樣本的 “盲區” 問題。

2. 倒置光片顯微鏡
樣本掛載:類器官置于 V 型 FEP 孔中,底部鋪薄層高濃度 ECM 凝膠(5μL Matrigel)。
成像參數:采用 20× 水浸物鏡,雙光片照明,z 軸步長 1μm。

04分析結果
乳腺類器官發育動態:
單細 - 胞來源的乳腺類器官(H2B-mCherry 核標記),光片成像清晰記錄分支延伸速度(平均 2.5μm/h)和方向,發現分支優先向 ECM 凝膠疏松區域生長,提示基質硬度影響發育方向。
藥物 / 因子處理響應:
加入 2.5nM FGF2 后,乳腺類器官分支數量在 6 天內增加 3 倍,光片成像追蹤到 FGF2 誘導的 “頂端細胞增殖 - 基底細胞遷移” 協同過程;而加入 ERK 抑制劑后,分支延伸停滯,且頂端細胞 ERK 活性降至基線水平,驗證了 ERK 信號的關鍵作用。
成像質量與光毒性:
連續 72 小時成像后,乳腺類器官的存活率仍保持 80% 以上(Live-or-Dye 壞死標記率 < 5%),遠高于共聚焦顯微鏡(48 小時存活率 < 50%),證明光片顯微鏡的低光毒性優勢;且成像分辨率足以區分單個細胞的核形態(如成纖維細胞的細長核 vs 上皮細胞的圓形核)。
多類型類器官通用成像 ——
果糖 - 甘油透明化與光片技術的普適方案
01文獻簡介
發表于《Nature Protocols》(2019)的《High-resolution 3D imaging of fixed and cleared organoids》,提出了一套適用于人腸道、肝臟、乳腺、氣道、腎臟類器官的通用 3D 成像 protocol。研究團隊研發了低毒性、高透明效果的 “果糖 - 甘油透明化試劑”,結合共聚焦、多光子和光片顯微鏡,實現從細胞骨架到亞細胞結構的高分辨率成像,且透明化樣本可長期存儲,為不同來源類器官的標準化成像提供了 “操作手冊” 級方案,已被廣泛應用于疾病建模和藥物篩選研究。

02組織透明化方法
該研究的核心創新是果糖 - 甘油(FG)透明化試劑,具體配方與流程具有普適性:
1.透明化流程:
PFA固定:類器官經 4% PFA 固定 45 分鐘(囊性類器官可縮短至 30 分鐘,避免塌陷),用含 0.1% Tween 20 的 PBS(PBT)清洗 3 次。
免疫標記:(一抗 4℃孵育過夜,二抗 4℃孵育過夜),用器官清洗緩沖液(OWB:含 1% BSA、0.1% Triton X-100 的 PBS)充分清洗,去除未結合抗體。
透明化處理,室溫孵育 20 分鐘,即可成像;若需存儲,可直接置于 - 20℃,6 個月內熒光信號無顯著衰減。
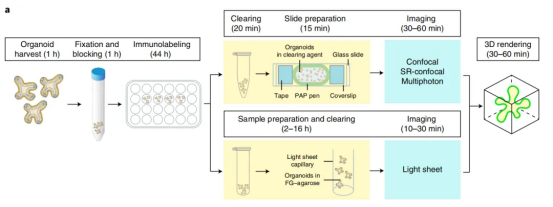
2.優勢對比:
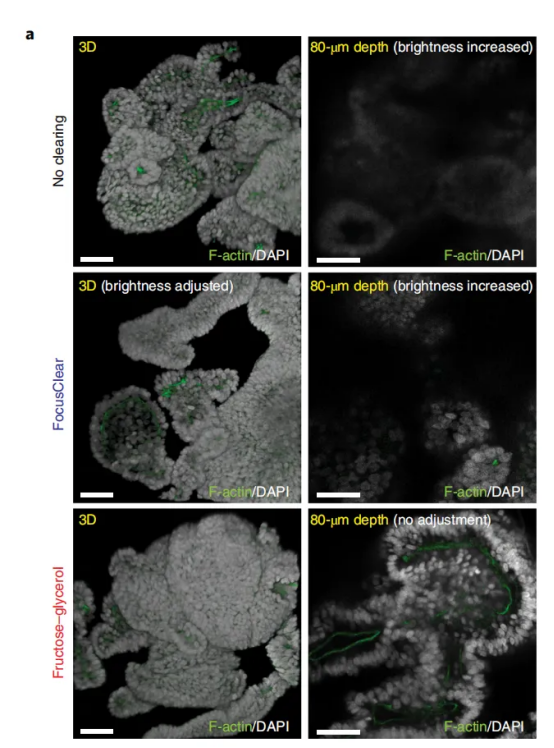
類器官透明化后的 DAPI 熒光強度高 3 倍,且透明化后類器官無收縮。
與無透明化相比:可使成像深度提升 2 倍(無透明化僅能穿透 100μm vs 透明化可穿透 200-500μm),且深層細胞的信號強度衰減率降低 50%。
03光片顯微鏡成像方法
研究針對不同類器官特性,適配光片顯微鏡(Zeiss Light Sheet Z.1) 的標準化方案:
樣本掛載(光片專用):
類器官與低熔點瓊脂糖(0.4%)+ FG 試劑混合(40℃下制備),吸入玻璃毛細管(直徑 1.5mm),4℃冷卻凝固后,將毛細管置于光片成像 chamber 中,chamber 內填充 FG 試劑,避免樣本脫水。
成像參數:
10×(NA 0.2)和檢測物鏡 20×(NA 1.0,適配 透明化試劑的折射率),光片厚度 6μm,雙光片照明以減少陰影,z 軸步長 1-2μm,根據類器官大小調整成像范圍(腸道類器官需 z 范圍 500μm,氣道類器官需 300μm)。


多模態兼容:
若類器官含熒光報告基因(如 H2B-mNeonGreen),可直接成像;若需免疫標記,可在透明化前完成,透明化過程不影響抗體結合效率(如 E - 鈣粘蛋白標記率與未透明化組一致,均為 95% 以上)。

04分析結果
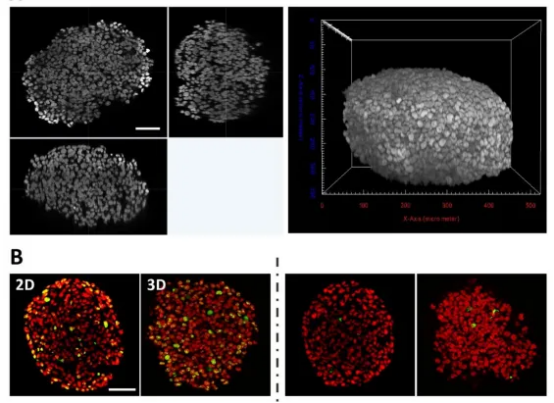
| 三維可視化:組織透明化后類器官三維成像相較于二維成像的優勢,能夠清晰呈現類器官樣本的關鍵結構特征。
| 成像深度與熒光強度加深:透明化步驟后,與未進行透明化處理的樣本相比,類器官成像的熒光強度顯著增強,且 z 軸方向的成像穿透深度也有所提升。
| 3D細胞亞型定量分析:能夠支持細胞分割算法對整個類器官中細胞的數量以及不同細胞亞型中各類細胞標志物的存在情況進行定量分析

類器官組織透明化解決方案
01組織透明化的高深度、高質量,高通量類器官平臺
快速透明化—僅需5-10min即可透明化500um 厚的樣品
溫和光學透明化—對熒光標記組織進行透明化用于 3D 成像后,對檢測靈敏度或樣品形態的影響小
工作流程兼容性—無需其他設備或儀器即可輕松實現
平臺兼容性—與大多數熒光染料和標準熒光成像儀器兼容
光片顯微平臺—實現高分辨類器官三維可視化

02組織透明化相關產品

免責聲明
客服熱線: 15267989561
加盟熱線: 15267989561
媒體合作: 0571-87759945
投訴熱線: 0571-87759942

下載儀表站APP

Ybzhan手機版

Ybzhan公眾號

Ybzhan小程序